 Postpunkční syndrom je soubor pacientem nepříjemně vnímaných příznaků, které vznikají po lumbální punkci nebo aplikaci epidurální anestezie. Hlavní potíží pacienta je bolest hlavy – tzv. pospunkční cephalea nebo chcete-li anglicky postdural puncture headache.
Postpunkční syndrom je soubor pacientem nepříjemně vnímaných příznaků, které vznikají po lumbální punkci nebo aplikaci epidurální anestezie. Hlavní potíží pacienta je bolest hlavy – tzv. pospunkční cephalea nebo chcete-li anglicky postdural puncture headache.___
___
1. Definice a klinické příznaky postpunkčního syndrom
Postpunkční bolest hlavy – cefalea (postdural puncture headache, PDPH) vzniká jako následek perforace dura mater a arachnoidey v souvislosti s předchozí punkcí epidurálního, resp. subarachnoidálního prostoru.
Bolest jeví souvislost s polohou postiženého. Začíná vsedě nebo vestoje, zhoršuje se při kašli i při malých pohybech. Úleva nastává vleže na zádech. Bolest hlavy má obvykle charakter tupého tlaku v záhlaví, který se rozšiřuje přes temeno hlavy do oblasti čela a do očí. Připojuje se reflexní spazmus krčního a zádového svalstva, pseudomeningismus. Většina postižených udává důležitý anamnestický údaj, že podobnou bolest hlavy ještě nikdy nezažili.
Vznik bolestí bývá vzácně okamžitý, většinou nastává s odstupem několika dní po punkci. Průměrně dochází k příznakům 48 hodin po punkci. Délka obtíží se popisuje od několika hodin do několika měsíců, největší intenzita bolestí trvá v průměru 4 dny, pak bolest zpravidla spontánně, avšak pomalu odezní. K dalším přidruženým symptomům patří nauzea, vomitus, deprese, změny vidění a sluchu.
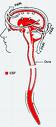
Triáda symptomů cefalea, oční poruchy a sluchové poruchy nese název “syndrom ze snižování intrakraniálního tlaku” (obr. 1).
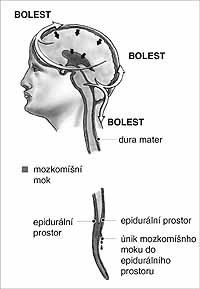
Pokles tlaku mozkomíšního moku v subarachnoidálním prostoru. Únik tekutiny perforačním otvorem do epidurálního prostoru.
Poruchy zraku souvisejí s tahem za VI. hlavové nervy (nn. abducentes), který vzniká při poklesu tlaku v cerebrospinálním moku (obr. 2). Poruchy sluchu mohou vzniknout s poklesem tlaku v moku anebo v důsledku anatomické komunikace mezi endolymfatickými kanálky vnitřního ucha a prostorem obsahujícím cerebrospinální mok.
Bolest hlavy nemusí být vždy následkem perforace dura mater. Existují i jiné závažné příčiny, za které je možno postpunkční cefaleu zaměnit.
Diferenciální diagnostika postpunkčního syndromu:
- meningitis,
- intra-, extra- nebo subdurální hematom,
- postižení mozku infarktem (trombóza mozkových vén jako následek změn nitrolebečního tlaku vlivem epidurální nebo subarachnoidální aplikace roztoku),
- hypertenzní krize,
- migréna,
- metabolické změny (hypoglykémie, rozvrat elektrolytů),
- poporodní psychické změny,
- hormonální změny,
- spondylogenní bolesti krční páteře jako důsledek nepohodlné polohy na operačním stole.
Stanovení diagnózy cefaley, která nesouvisí s postpunkčním syndromem:
- anamnéza rodinná i osobní: časté bolesti hlavy,
- depresivní syndrom.
Fyzikální vyšetření u postpunkčního syndromu:
- teplota, krevní tlak, vyšetření srdce a plic,
- celkové interní vyšetření,
- neurologické vyšetření.
Laboratorní vyšetření:
- hematologické vyšetření, biochemické vyšetření krve,
- kontrola glykémie,
- EKG,
- vyšetření počítačovým tomografem, při negativním nálezu vyšetření s kontrastní látkou nebo magnetickou rezonancí.
2. Patofyziologie postpunkčního syndromu
Postpunkční cefalea má složitou a multifaktoriální etiologii. Za normálních okolností se mozek i mícha “vznášejí” v mozkomíšním moku uzavřeném v obalu mozkomíšních plen. Takto je CNS spolehlivě chráněn před mechanickými inzulty. Normální tlak mozkomíšního moku v lumbální oblasti činí 5–15 cmH2O (0,5–1,5 kPa), měřeno vleže, vestoje stoupá přes 40 cmH2O (4 kPa), kdežto tlak v epidurálním prostoru v případě obou poloh zůstává téměř nezměněn a je téměř shodný s tlakem atmosferickým. Proto má při vztyčené poloze (tlakový rozdíl činí 40–50 cmH2O, tj. 4–5 kPa) mok větší tendenci unikat do extradurálního prostoru. Mnohé studie upozorňují na vztah mezi symptomy postpunkční cefaley a redukcí objemu, a tím i tlaku mozkomíšního moku, syndrom likvorové hypotenze. Kunkle se spolupracovníky popisuje symptomy cefaley ve vzpřímené poloze již při úniku 20 ml moku. Základní příčina postpunkční bolesti hlavy spočívá v perforaci míšních obalů a následném snížení tlaku mozkomíšního moku, protože mok uniká z intratekálního prostoru do prostoru extradurálního.
Akutní zmenšení objemu mozkomíšního moku má vliv na mozkovou tkáň. Dochází k trakci anatomických struktur, které způsobují bolest – intrakraniální siny, cévy a nervy a dále tentorium. Změnami napětí tentoria dochází k iritaci n. trigeminus, n. abducens (zejména), n. glossopharyngeus, n. vagus a event. prvních tří krčních nervů.
Symptomy se zmenšují nebo ustupují po uložení pacientky do vodorovné polohy nebo po arteficiálním zvýšení tlaku mozkomíšního moku nebo po jeho substituci fyziologickým roztokem subarachnoidální injekcí. Léčebný efekt přináší i komprese břicha pevným obvazem (korzetem) na dobu cca 24 hodin, avšak tento mechanický manévr je pro nedělku značně nepohodlný až nepříjemný. Úpravy tlaku mozkomíšního moku je možné dosáhnout zvýšením tlaku v epidurálním prostoru aplikací vhodného roztoku (fyziologický roztok nebo koloid) nebo autologní krve.
Dalším zdrojem bolesti je cévní dilatace v intrakraniální oblasti. Intrakraniání tlak v neměnném kostním intrakraniálním prostoru je určen objemem všech tří kompartmentů: objem krve v mozku tvoří 5–8 %, nervová tkáň mozku činí 85 % a objem mozkomíšního moku činí 7–10 %.
Snížení objemu moku vyvolá reflexní dilataci mozkových cév, a tím i zvýšení podílu krve v mozku. Zmenšení objemu (tlaku) jednoho kompartmentu vyvolá symetrickou změnu objemu (tlaku) u zbývajících složek intrakraniálního prostoru. Vazodilatace v mozku vyvolává dráždění perivaskulárních nociceptivních receptorů, které způsobují bolesti připomínající bolesti hlavy charakterické pro migrénu.
Incidence postpunkční bolesti hlavy u těhotných žen a u žen v šestinedělí je zhruba 2x vyšší než u ostatní populace. Vyšší incidence je vyvolána multifaktoriálními vlivy. Ženy v peripartálním období jsou náchylné ke změnám intravaskulárního objemu a k dehydrataci (krevní ztráta, omezený příjem tekutin v průběhu porodu, zvýšená diuréza po porodu), mají sklon k nauzee a ke zvracení. Uvedené faktory způsobují pomalejší regeneraci mozkomíšního moku. Během porodu přechodně stoupá intratekální tlak. Zvýšený abdominální tlak během těhotenství vede k vyšší distenzi epidurálních cév, což na jedné straně způsobuje zmenšení epidurálního prostoru, na druhé straně zvýšení tlaku tohoto prostoru na mozkomíšní obaly. Po porodu, po odlehčení tlaků na cévní systém v dutině břišní, dochází k rychlé normalizaci cévního, zejména žilního systému a objem v epidurálních cévách klesá. Tím klesá i tlak v epidurálním prostoru, zvyšuje se gradient tlaků mezi intra- a extradurálním prostrorem, a tedy náchylnost k úniku moku při perforaci dura mater.
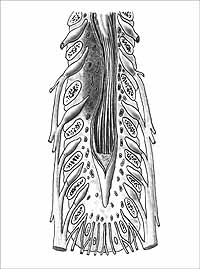
Postpunkční bolesti hlavy jsou běžně považovány za komplikaci punkce subarachnoidálního prostoru. Cefalea nedělku nebo operantku sice obtěžuje, někdy i dlouhodobě, ale ve své podstatě se jedná v naprosté většině případů o komplikaci nezávažnou. Vzácnou, nicméně potenciálně letální komplikací je krvácení z přemosťujících cév do subarachnoidálního prostoru mozku (obr. 3). Jeho nebezpečí spočívá v tom, že bolest hlavy (jindy alarmující symptom intrakraniálního krvácení) zůstane nepoznána, resp. je zaměňována za postpunkční cefaleu, a subarachnoidální krvácení může vyústit i letálně.
3. Prevence postpunkčního syndromu
Nejlepší prevencí postpunkční bolesti hlavy je provádění epidurální/subarachnoidální punkce tenkými a velmi tenkými jehlami a to metodou atraumatické lumbální punkce. Postpunkční bolest hlavy nejčastěji vzniká při nezdařené detekci epidurálního prostoru jako následek perforace tvrdé pleny a pavučnice Tuohyho jehlou. Zde pak spočívá prevence v dokonalém technickém provedení úkonu. Určitý podíl nezdarů však zcela vymýtit nelze.
V případě subarachnoidálních blokád hrají roli následující faktory:
Průměr jehly: incidence postpunkční cefaley klesá s průměrem punkční jehly. Incidence cefaley u extrémně tenkých jehel o průměru 29–32 G je zanedbatelná.
Směr vpichu: mnoho autorů již dlouhou dobu upozorňovalo na souvislost postpunkční cefaley se směrem průniku punkční jehly. Mihic popisuje pokles incidence cefaley z 16,1 na 0,24 %, pokud volíme šikmý průnik do subarachnoidálního prostoru namísto přímého (kolmého).
Hrot jehly: jehly s obvyklým úkosem břitu (typu Quincke) způsobují větší trauma dura mater než jehly s konickým hrotem (např. pencil-point typu Whitacre nebo Sprotte). V dnešní době je na trhu bohatá nabídka jehel, které jen v malé míře traumatizují tkáň míšních obalů, takže jejich použití způsobuje jen malý únik likvoru.
Úhel vpichu, pod kterým se jehlou proniká plenami, má vliv na velikost a trvání otvoru. Při šikmém úhlu průniku vzniká po vyjmutí jehly ventilový mechanismus, který následně úniku likvoru brání. Paramediánní směr průniku míšními obaly přispívá k významnému snížení výskytu postpunkční cefaley.
Poloha rodičky/pacientky: subarachnoidální analgezie/anestezie se běžně podává vleže na boku, když je rodička/pacientka maximálně flektována v zádech (tzv. kočičí hřbet). Tato poloha způsobuje napětí ve tkáni míšních plen a otvor po jehle může v extenzi, resp. po narovnání a uložení na záda, mít jiný, pro únik moku méně výhodný tvar, než kdybychom vpich provedli v méně flektované pozici.
Použité agens: dlouho se tradovalo, že látka podaná do subarachnoidálního prostoru nemá vliv na postpunkční cefaleu. Naulty se spolupracovníky však v roce 1985 popisuje vliv roztoku lokálního anestetika na postpunkční cefaleu a popisuje následující vztah ke vzestupu její incidence: lidokain, bupivakain, tetrakain a prokain. Zdá se, že použití lokálního anestetika s glukózou snižuje cefaleu. Další autoři popisují, že přidání adrenalinu nebo fentanylu snižuje incidenci postpunkční cefaley.
Kontinuální katetrizace subarachnoidálního prostoru: kontinuální subarachnoidální přístup se zavedeným katétrem není dnes používán často. Zejména v porodnictví tento přístup téměř postrádá odůvodnění, protože rizika převyšují výhody.
Byla však vyvrácena dřívější hypotéza, že zavedení velmi tenkého katétru zvyšuje výskyt postpunkční cefaley. Řada autorů podala důkazy, že katétr procházející mozkomíšními obaly nezvyšuje výskyt postpunkční cefaley. Naopak nižší výskyt této komplikace je pravděpodobně způsoben zánětlivou reakcí okolo místa vpichu s tvorbou edému, což po vytažení katétru přispívá k rychlé tvorbě fibrinové zátky. Zundert řešil u porodu případy nechtěné perforace míšních obalů Tuohyho jehlou zavedením katétru a pokračováním subarachnoidální analgezie. Postpunkční cefalea vznikla pouze v 37 % případů.
4. Léčba postpunkčního syndromu
Nastane-li nechtěná perforace míšních obalů, je třeba rodičku zvlášť pečlivě sledovat. Podle vlastní zkušenosti navrhuji tento postup:
- je třeba zajistit, aby údaje v dokumentaci rodičky nebo v dokumentaci o průběhu šestinedělí byly přesné (místo perforace, průměr jehly, dokumentace dalšího postupu – využití otvoru v míšních obalech pro subarachnoidální analgezii, volba jiné intervertebrální štěrbiny atd.), záznam o případných nesnázích při provádění punkce;
- není třeba ženu na možnou komplikaci ihned upozorňovat. Bolest hlavy a zad je po porodu relativně častá stížnost nedělek a mohlo by dojít ke vsugerování obtíží;
- naopak personál oddělení šestinedělí, zejména zdravotní sestry, je třeba na možnost vzniku postpunkční bolesti hlavy předem upozornit; jakmile si nedělka začne stěžovat, jsou sestry povinny tuto skutečnost ohlásit neprodleně příslušnému lékaři, nejlépe přímo anesteziologovi;
- lékař s pacientkou pohovoří a srozumitelně jí vysvětlí pravděpodobnou příčinu obtíží. Přesto, že intenzita obtíží dosahuje někdy dramatických rozměrů, žena musí pocítit, že zdravotnický personál zná původ bolestí. Dále následuje určování diagnózy a po jejím potvrzení příslušná terapie.
Konzervativní postup se používá vždy na prvním místě, protože často již sám o sobě pomáhá snižovat intenzitu postpunkčních obtíží:
- první pravidlo konzervativního postupu spočívá v poloze nedělky, a to na rovné posteli a na zádech;
- pokud přes tuto polohu nepociťuje žena úlevu, není třeba dále toto pravidlo striktně dodržovat; dlouhodobější imobilizace totiž zvyšuje výskyt nauzey a může být příčinou trombembolické nemoci. Na druhé straně, pacientka se naučí většinou sama polohu na zádech vyhledávat a zaujímat, protože tak pociťuje ústup obtíží, jedná se o úlevovou polohu;
další kroky v konzervativním přístupu jsou:
- perorální a intravenózní hydratace nedělky (pokus o zvýšenou produkci mozkomíšního moku),
- analgezie (běžná analgetika, nesteroidní antirevmatika, NSAID): jako výhodná se jeví kombinace NSAID a centrálního myorelaxancia. Někteří autoři doporučují kompresi břicha a lumbální oblasti. Nepohodlí ženy při tomto postupu bylo již výše zmíněno. Komprese komplikuje i péči o dítě a zejména představuje zvýšené riziko trombembolie ze sníženého žilního návratu. Ostatně tato léčba není ani příliš účinná.
Kofein a teofylin: někteří autoři doporučují i.v. podání kofeinu v dávce až 500 mg opakovaně. Popisují zkrácení délky a snížení intenzity bolesti. Jiní autoři popisují po podání 300 mg kofeinu p.o. a 300 mg teofylinu p.o. přechodný vzestup intenzity obtíží a s časovým odstupem teprve úlevu. Podstatou této léčby je vazokonstrikce dilatovaných cév v mozku.
Infúzní terapie: klinické studie s podáním jednorázové dávky nebo kontinuální infúze fyziologického roztoku do epidurálního prostoru prokazují významný vliv na úlevu od bolestí hlavy. Tlak infúzního roztoku v epidurálním prostoru pomáhá vyrovnávat tlakový rozdíl mezi tlakem v durálním vaku a epidurálním prostoru, a tím se pomáhá snižovat únik mozkomíšního moku. Bohužel účinek tohoto postupu bývá pouze přechodný, cefalea se často navrací.
Epidurální “krevní plomba” neboli “krevní zátka” (epidural blood patch): Gormley jako první popsal v roce 1960 podání autologní krve do epidurálního prostoru jako způsob léčby postpunkční cefaley. Dnes je tento zákrok pro svoji až 90% účinnost hojně využíván.
Krevní plomba spočívá v aplikaci asi 10–15 ml autologní, čerstvé krve bez protisrážlivých činidel nejlépe v místě předchozí neúspěšné punkce (řádné vedení anesteziologické dokumentace). Vynikající účinnost této metody spočívá v rychlém zvýšení tlaku v epidurálním prostoru, ve vyrovnání tlakového spádu a v trvalém zakrytí otvoru v tvrdé pleně koagulovanou a později organizovanou krví (obr. 4).
Tzv. krevní plomba v epidurálním prostoru
Jelikož tlak v epidurálním prostoru je v této situaci vždy pozitivní, nelze využít k detekci vizuální metodu (“vtažená kapka”), ale pouze metodou “ztráty odporu”. Asistující osoba hned nato nabere samostatnou stříkačkou čerstvou žilní krev nedělky, kterou punkci provádějící anesteziolog bez prodlevy podá do epidurálního prostoru. Je-li zaveden katétr, je možné jej použít k aplikaci krve, avšak tento postup může pro vysokou viskozitu krve selhat. Manévr usnadníme, pokud katétr zkrátíme na cca 10 cm . Protože však katétr může být po předchozím použití kontaminován a krevní depo představuje živnou půdu pro rozvoj infekčního procesu, není možno tento postup považovat za zaručeně bezpečný.
Krev je oproti fyziologickému roztoku viskóznější a má vyšší osmotický tlak, takže se resorbuje pomaleji než fyziologický roztok.
Výkon zpravidla vyvolá okamžitou a často trvalou úlevu. Jindy pominou bolesti do 1–2 dnů. Při obnově obtíží je možné výkon opakovat. Nedojde-li k úlevě ani pak, je žádoucí uvažovat o jiné příčině. Zejména je třeba vyloučit krvácivý nebo trombotický proces v CNS. Do vyřešení problému musí být pacientka pečlivě sledována ve zdravotnickém zařízení.
Možnou alternativou je podání dextranu (Rheodextran infusia 10%).
Profylaktické, bezprostřední nebo časné podání “krevní plomby” bylo sice navrženo, avšak tento postup nebyl k rutinnímu užití všeobecně přijat. U cca 15 % nedělek se postpunkční syndrom nevyvine. Jindy můžeme vystačit s konzervativním a farmakologickým postupem. Práce autorů, kteří podávali “krevní plombu” profylakticky, významné ovlivnění cefaley neprokázaly.
Aplikace “krevní plomby” může navodit přechodný pocit tupého tlaku v místě podání nebo parestezie typu kořenového dráždění v místě vpichu. Vzácně byl popsán meningismus, jindy břišní křeče, pískání v uších, závratě, horečnatý průběh a hematom v anatomických strukturách, blízko kterých byla krev podána.
Adheze (následek postupné organizace hematomu) mezi lig. flavum a dura mater nebyly popsány, a to ani u těch pacientek, kde byla po “krevní plombě” v anamnéze později provedena z jiné indikace neurochirugická laminektomie. Griffiths popsal v roce 1993 zobrazení “krevní plomby” pomocí magnetické rezonance a upozornil, že krev může unikat meziobratlovými otvory, což se pokládá za vysvětlení zmíněného kořenového dráždění. Dále popsal kompresi durálního vaku a tamponádu perforačního otvoru v míšních plenách. Krev se po podání šířila spíše kraniálně. Krev byla popsána i v subarachnoidálním prostoru, což dále vysvětluje opět dočasné známky meningeálního dráždění.
Kontraindikace “krevní plomby” představuje septikémie nebo lokální infekce v místě vpichu, poruchy koagulace a akutní rozvoj neurologických poruch míchy. Na druhé straně je možné výkon úspěšně provést i u HIV pozitivních pacientek. Podání “krevní plomby” není kontraindikací pro podání epidurální nebo subarachnoidální analgezie/anestezie v pozdějším období. Krev se z epidurálního prostoru resorbuje za několik dní.
Pacientkám, které z náboženských nebo jiných důvodů odmítají podání “krevní plomby”, je možné navrhnout jinou alternativu, např. 20 ml dextranu (Rheodextran infusia 10%) nebo jiného koloidního roztoku. Tato léčba má ovšem podstatně větší podíl selhání.

